作为“临床研究综合服务一体化的创新型CRO”,兴德通深耕创新药领域,在创新药研发、临床研究及成果转化的实践中积累了丰富的经验,在细胞基因治疗产品的开发、注册申报和临床研究中均有成功案例,兴德通已成为细胞基因治疗领域头部CRO。4月22日,兴德通受邀参加在北京举办的第五届北京生物药工艺开发大会。会上,兴德通分享了细胞药物临床研究及注册申报的技术要点和解决方案,得到与会嘉宾的热烈反响。
兴德通副总经理、细胞临床研究中心主任张爱玲受邀出席大会细胞治疗专场论坛,发表了《我国干细胞新药临床试验进展情况及审评关注点分析》主题演讲。张爱玲副总分享了兴德通在细胞基因治疗领域中的前瞻布局,介绍了兴德通多款细胞药物IND申报及顺利开展临床试验的成功案例,备受与会嘉宾的关注与好评。
目前,兴德通承接了四十余项细胞基因治疗研究项目,已积累细胞治疗药物开发经验,成功辅助多款细胞新药获批IND、并顺利开展临床研究,辅助2款细胞产品进入Ⅲ期临床试验。张爱玲副总结合兴德通CGT产品研究经验,讲解了国内外干细胞产品监管状况,详细介绍了我国对干细胞产品的监管情况,点明了在不同国家进行干细胞产品注册申报时应遵循的指导原则和法规,帮助指导干细胞产品注册申报,帮助企业节省时间和成本。
张爱玲副总深入交流了干细胞从科研到产品的考量、干细胞注册申报中的常见问题。仔细梳理了干细胞注册申报的流程、申报资料的关注重点,强调了干细胞药学申报资料中的常见问题、CMC策略及审评关注点、非临床策略及审评关注点、临床策略及审评关注点,还简明扼要地分析了干细胞IIT成果用于IND的前置条件、干细胞IIT到IND的衔接设计。演讲内容详实丰富,具有较强的实践指导意义,有利于帮助业内在进行干细胞研究和注册申报时少走弯路、加快研发进程。
大会期间,参会嘉宾们与张爱玲副总进行了深入的交流探讨,共同展望细胞基因治疗产品的研发前景。
兴德通在实践中总结细胞治疗产品研发过程中的共性问题,在细胞团体标准、干细胞临床试验质量控制体系、细胞IIT数据应用到IND申报的临床研究管理体系等多方面发力,提供高效解决方案。
未来,兴德通将持续发挥细胞临床研究引领作用、保持领先地位,以“专精特新”CRO不断创新,为医药健康产业提供重要的产业链配套服务,不断推进细胞基因治疗产品的高质量临床研究,践行创新“ICVP”模式,为促进细胞治疗产业发展持续长久地发力,不断推动医药创新高质量发展。
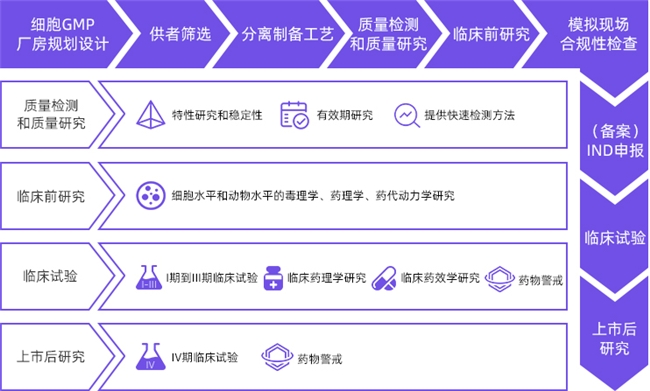
图丨兴德通提供涵盖细胞治疗产品开发的全产业链服务
兴德通已用专业高效的CRO执行力助推多项干细胞临床研究在国内科研实力雄厚的临床试验机构顺利开展。兴德通拥有细胞领域经验丰富的专业人员、团队、从业背景等标准配置,有强大的产品开发策略与注册转化能力,对细胞研究新法规具有敏锐的洞察力和分析能力。CRO团队严格按照标准操作规程SOP执行,保障临床试验顺利开展。
兴德通为企业提供GMP厂房建设与咨询、非临床实验设计及临床研究项目运营和管理等细胞治疗产品研发全产业链完整解决方案,还可帮助企业模拟现场合规性检查,帮助企业少走弯路,加快细胞治疗产品上市。